 关注我们
关注我们


2026年3月27日,《自然·医学》(IF=50) 发表了由我院吴一龙教授领衔的”比较 ONC-392 与多西他赛治疗经 PD-1/PD-L1 抑制剂治疗后进展的转移性非小细胞肺癌受试者的两阶段、随机对照多中心 III 期临床研究”PRESERVE-003第一阶段结果。该研究公布了新型CTLA-4抑制剂Gotistobart(BNT316/ONC-392)在既往接受过PD-(L)1抑制剂联合化疗后进展的肺鳞癌患者中的疗效与安全性。
过去,肺鳞癌患者在免疫联合化疗失败后,二线治疗选择极为有限。多西他赛作为二十余年未变的标准二线治疗,疗效有限且毒性明显,中位总生存期仅为8.0至9.4个月。尽管近年来多项新型疗法,包括抗体药物偶联物(ADC)、酪氨酸激酶抑制剂(TKI)联合免疫等,对比多西他赛的探索均未取得阳性结果,但PRESERVE-003研究打破了这一僵局。
本次报告的PRESERVE-003第一阶段中87例患者(Gotistobart组45例,多西他赛组42例)的结果(如下图),经过中位14.5个月的随访,研究取得了突破性发现:
1. 总生存期显著延长:Gotistobart组中位OS尚未达到(95% CI 9.3个月至未评估),而多西他赛组为10.0个月(95% CI 6.2–11.9个月),风险比(HR)为0.46,死亡风险降低54%(HR=0.46,P=0.0102)。12个月OS率翻倍,Gotistobart组为63.1%,多西他赛组仅为30.3%。
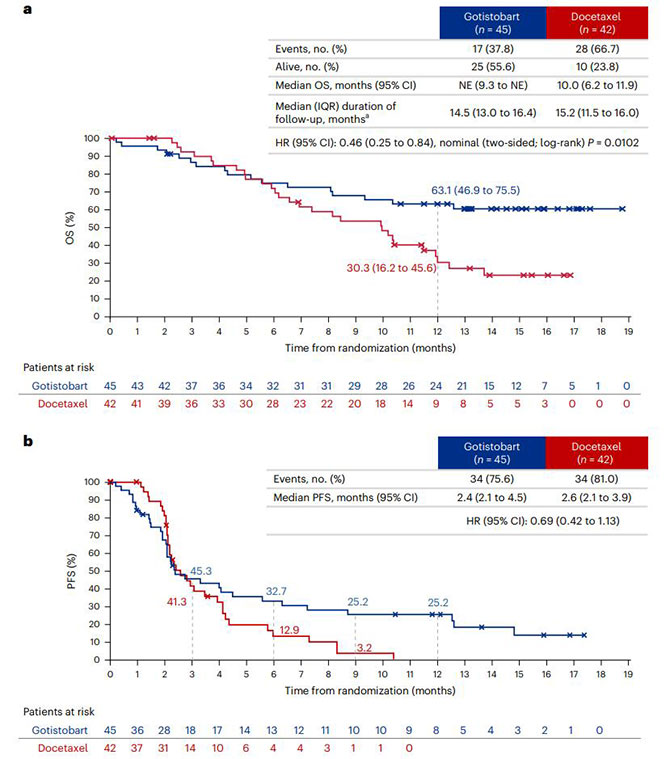
2. 客观缓解率提升,缓解持续时间更长:Gotistobart组的客观缓解率(ORR)为20.0%,而多西他赛组仅为4.8%。缓解持久性方面,Gotistobart的中位缓解持续时间(DoR)达11.0个月,远超多西他赛的3.8个月。尽管两组中位无进展生存期(PFS)相近(2.4个月 vs 2.6个月),但Gotistobart在长期随访中呈现“尾部效应”,提示Gotistobart患者得到长期获益。
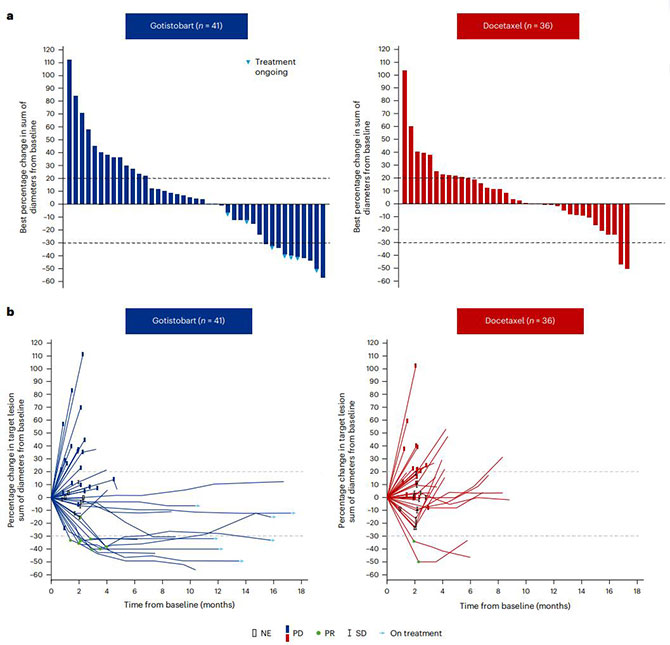
3. 安全性可控,停药率可接受:Gotistobart组≥3级治疗相关不良事件发生率为42.2%,低于多西他赛组的48.8%。因不良反应永久停药的患者比例为13%,未发生治疗相关死亡事件。最常见的不良反应为腹泻、结肠炎和ALT升高,管理策略成熟。
基于第一阶段结果,PRESERVE-003研究的关键性第二阶段仍在进行中。本研究的Leading-PI吴一龙教授表示,若最终结果一致,有望进一步验证Gotistobart的临床价值,并推动其成为晚期肺鳞癌后线治疗的新标准。
甘彬